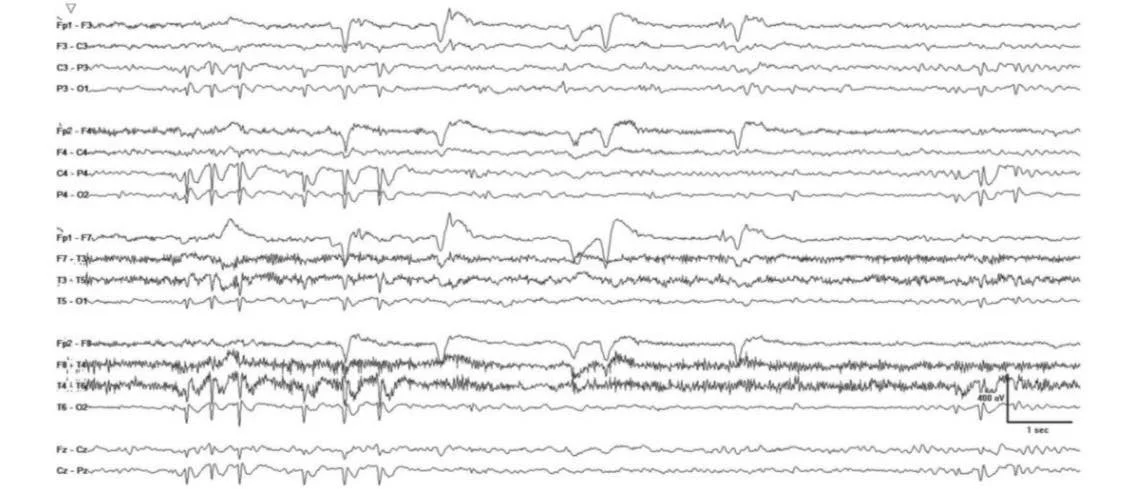
Các mẫu hình qEEG trong động kinh do gen”
Thảo luận từ nghiên cứu của Galer và cộng sự (Neurology, 2025)
1) Vì sao qEEG quan trọng ngay lúc này?
EEG là công cụ lâu đời và được dùng hằng ngày. Tuy nhiên, ngay cả trong kỷ nguyên y học gen, phần lớn diễn giải EEG vẫn dựa vào đọc bằng mắt (visual inspection) — tức chúng ta nhìn sóng và mô tả.
Câu hỏi nghiên cứu: Liệu thông tin “ẩn” trong EEG có thể được đo một cách khách quan, lặp lại được, và từ đó phân biệt các nhóm động kinh di truyền như STXBP1, SCN1A, SYNGAP1 hay không?
Nếu đo được khách quan và tái lập, qEEG có thể tiến một bước quan trọng: từ “mô tả định tính” trở thành biomarker/endpoint cho nghiên cứu và thử nghiệm lâm sàng.
2) Có thể tìm thấy “tín hiệu” nào trong “nhiễu”?
Nhóm nghiên cứu dùng các phương pháp học máy để tìm “tín hiệu” trong dữ liệu EEG đời thực.
(A) Học máy giúp chỉ ra “đặc trưng nào quan trọng” để phân biệt theo gen
Mục tiêu là trích xuất các qEEG features quan trọng nhất giúp phân biệt nhóm chứng với các nhóm STXBP1 / SYNGAP1 / SCN1A.
(B) Một chỉ số đơn giản nhưng hữu ích: global alpha–delta ratio
Alpha–delta ratio là chỉ số qEEG đã được nghiên cứu trước đó. Khi phân tích theo nhóm tuổi và nhóm bệnh, họ ghi nhận:
• STXBP1: khác biệt rõ so với chứng và nổi bật xuyên nhiều nhóm tuổi.
• Các nhóm khác (ví dụ SCN1A): khác biệt có ý nghĩa chỉ xuất hiện ở một số giai đoạn tuổi nhất định.
Ý nghĩa:
qEEG có thể có chữ ký theo gen, nhưng tuổi phát triển là yếu tố điều biến cực mạnh. Và trong chỉ số này, STXBP1 có vẻ cho tín hiệu đều và mạnh hơn.
3) biến EEG thành dữ liệu
Một điểm quan trọng của công trình là cách tiếp cận:
mọi EEG lâm sàng vốn đã là dữ liệu số, nên hoàn toàn có thể “lấy lại để phân tích lại” một cách hệ thống.
Nhóm nghiên cứu xây dựng một pipeline tự động có thể:
• clean (làm sạch),
• segment (chia đoạn),
• quantify (định lượng)
trên hàng ngàn EEG lấy từ hồ sơ bệnh án điện tử (EMR).
Sau đó, họ trích xuất spectral features (các đặc trưng phổ) — tức phân bố “power” theo các dải tần — và đặt câu hỏi:
các pattern này có khác nhau giữa các động kinh do gen và nhóm chứng phát triển điển hình hay không?
4) Dữ liệu “đời thực” là điểm mạnh
Toàn bộ EEG trong nghiên cứu là EEG thực hành thường quy, không phải EEG “chuẩn phòng lab”. Tác giả nhấn mạnh điều này vì:
• dữ liệu sẵn có và quy mô lớn,
• phản ánh đúng workflow lâm sàng,
• dù chấp nhận đi kèm với nhiễu, biến thiên, và không hoàn hảo.
Cỡ mẫu:
• 154 EEG: SCN1A
• 95 EEG: STXBP1
• 46 EEG: SYNGAP1
• 847 EEG chứng từ 806 người không động kinh
Dù dữ liệu đời thực “noisy”, nghiên cứu vẫn cho thấy có thể trích xuất tín hiệu đo được ở quy mô lớn. Đây là minh họa rõ ràng cho tiềm năng của nghiên cứu dựa trên EHR/EMR để tìm biomarker từ chính dữ liệu sinh ra trong thực hành hằng ngày.
5) Từ hứa hẹn đến thực dụng: vì sao hồi cứu là bước 1 hợp lý trong bệnh hiếm?
qEEG biomarkers được kỳ vọng vì chúng:
• khách quan,
• tái lập,
• có thể nắm bắt những khía cạnh của rối loạn mạng não mà đọc EEG bằng mắt có thể bỏ sót.
Nhưng trong bệnh hiếm, thu thập biomarker tiền cứu thường tốn nguồn lực lớn (thời gian, chi phí, nhân lực). Vì vậy, tái sử dụng EEG lâm sàng hồi cứu là một bước đi thực dụng:
dùng dữ liệu sẵn có như “bãi thử” để nhận diện chỉ số nào thực sự informative, trước khi đầu tư vào natural history studies hoặc clinical trials.
6) “Chữ ký điện sinh lý” theo gen và theo vùng giải phẫu
Một kết quả thú vị là các chữ ký qEEG thường “không ồn ào”, nhưng nhất quán.
Ví dụ:
• STXBP1: giảm frontal alpha–theta ratio.
Ngoài ra, các mô hình phổ có thể phân biệt EEG giữa STXBP1, SCN1A, SYNGAP1 với độ chính xác cao, kèm theo “dấu ấn không gian”:
• STXBP1: nổi bật ở vùng trán (frontal)
• SCN1A: nổi ở vùng đỉnh (parietal)
• SYNGAP1: nổi ở vùng chẩm (occipital)
Điều này củng cố một giả định quen thuộc trong lâm sàng: mỗi gen có thể tác động lên mạng não theo cách khác nhau — và ở đây, giả định đó được ủng hộ bằng bằng chứng định lượng.
7) EEG nói được gì và không nói được gì?
Đây là đoạn mình đánh giá rất “thực tế”:
• Trong dữ liệu đời thực, các spectral features không dự đoán tốt tần suất cơn (seizure frequency).
• Nhưng qEEG features lại tương quan với chức năng vận động thô (GMFM-66), và thậm chí tốt hơn mô hình chỉ dùng tuổi.
qEEG có thể phản ánh tổ chức mạng não / mức phát triển thần kinh tốt hơn là phản ánh “gánh nặng cơn” theo kiểu đếm số cơn. Do đó, nhóm tác giả đề xuất cần đánh giá sâu hơn mối liên hệ qEEG–developmental outcomes bằng dữ liệu tiền cứu chất lượng cao (như các chương trình STARR và ProMMiS).
Kết luận:
Tín hiệu có thể nằm trong nhiễu — nếu ta biết cách khai thác dữ liệu.
EEG lâm sàng không chỉ để “đọc” mà còn có thể trở thành nguồn dữ liệu định lượng giúp hiểu:
• quỹ đạo tiến triển bệnh,
• đáp ứng điều trị,
• và kết cục phát triển.
Nghiên cứu này giống một lời nhắc: trong hành trình đi từ EEG → keto → gen → điều trị chính xác, cuối cùng chúng ta vẫn cần quay lại nền tảng.
Điện não không phải “điểm xuất phát đã qua”, mà là một “nguồn dữ liệu” chưa được khai thác hết.